آخرین مطالب
امکانات وب
در ترمودینامیک ، یک فرآیند ایزنتروپیک یک فرآیند ترمودینامیکی ایده آل است که هم آدیاباتیک و هم برگشت پذیر است. [1] [2] [3] [4] [5] [6] انتقال کار سیستم بدون اصطکاک است و هیچ انتقال خالص گرما یا ماده وجود ندارد. چنین فرآیند ایده آلی در مهندسی به عنوان مدل و مبنای مقایسه برای فرآیندهای واقعی مفید است. [7]این فرآیند ایده آل است زیرا فرآیندهای برگشت پذیر در واقعیت رخ نمی دهند. در نظر گرفتن یک فرآیند به عنوان هم آدیاباتیک و هم برگشت پذیر نشان می دهد که آنتروپی اولیه و نهایی یکسان هستند، بنابراین، دلیل نامیده شدن آن ایزنتروپیک (آنتروپی تغییر نمی کند). فرآیندهای ترمودینامیکی بر اساس تأثیری که بر سیستم خواهند داشت نامگذاری می شوند (مثلاً هم حجمی: حجم ثابت، ایزنتالپیک: آنتالپی ثابت). حتی اگر در واقعیت لزوماً امکان انجام یک فرآیند همسانتروپیک وجود ندارد، ممکن است برخی از آنها به این صورت تقریبی شوند.
کلمه "ایسنتروپیک" را می توان به گونه ای دیگر تفسیر کرد، زیرا معنای آن از ریشه شناسی آن قابل استنباط است . این به معنای فرآیندی است که در آن آنتروپی سیستم بدون تغییر باقی می ماند. همانطور که ذکر شد، اگر این فرآیند هم آدیاباتیک و هم برگشت پذیر باشد، ممکن است رخ دهد. با این حال، این همچنین می تواند در سیستمی رخ دهد که در آن کار انجام شده روی سیستم شامل اصطکاک داخلی سیستم است و گرما به مقدار مناسب از سیستم خارج می شود تا اصطکاک داخلی را جبران کند تا آنتروپی بدون تغییر باقی بماند. [8] با این حال، در رابطه با جهان، آنتروپی جهان در نتیجه افزایش مییابد که مطابق با قانون دوم ترمودینامیک است.
فهرست
قانون دوم ترمودینامیک بیان می کند [9] [10] که
جایی که


برای فرآیندهای برگشت پذیر، یک تبدیل ایزنتروپیک با "عایق بندی" حرارتی سیستم از محیط اطرافش انجام می شود. دما متغیر مزدوج ترمودینامیکی نسبت به آنتروپی است، بنابراین فرآیند مزدوج یک فرآیند همدما خواهد بود ، که در آن سیستم از نظر حرارتی به یک حمام گرمایی با دمای ثابت متصل میشود.
فرآیندهای ایزنتروپیک در سیستم های ترمودینامیکی [ ویرایش ]
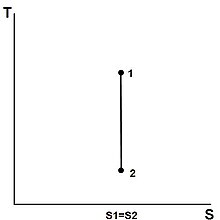
نمودار T-s (آنتروپی در مقابل دما) یک فرآیند همسانتروپیک، که یک قطعه خط عمودی است.
آنتروپی یک جرم معین در طول فرآیندی که به صورت داخلی برگشت پذیر و آدیاباتیک است تغییر نمی کند. فرآیندی که طی آن آنتروپی ثابت می ماند، فرآیند ایزنتروپیک نوشته شده نامیده می شود

بازده ایزنتروپیک دستگاه های جریان پایدار در سیستم های ترمودینامیکی [ ویرایش ]
اکثر دستگاه های جریان ثابت در شرایط آدیاباتیک کار می کنند و فرآیند ایده آل برای این دستگاه ها فرآیند ایزنتروپیک است. پارامتری که چگونگی تقریب کارآمدی یک دستگاه به دستگاه ایزنتروپیک مربوطه را توصیف می کند، راندمان ایزنتروپیک یا آدیاباتیک نامیده می شود. [13]
راندمان ایزنتروپیک توربین ها:
راندمان ایزنتروپیک کمپرسورها:
راندمان ایزنتروپیک نازل ها:
برای تمام معادلات بالا:



دستگاه های ایزنتروپیک در چرخه های ترمودینامیکی [ ویرایش ]
توجه: مفروضات ایزنتروپیک فقط برای چرخه های ایده آل قابل اجرا هستند. سیکل های واقعی به دلیل ناکارآمدی کمپرسور و توربین و قانون دوم ترمودینامیک تلفات ذاتی دارند. سیستم های واقعی واقعا ایزنتروپیک نیستند، اما رفتار همسانتروپیک تقریبی مناسب برای بسیاری از اهداف محاسباتی است.
جریان ایسنتروپیک [ ویرایش ]
در دینامیک سیالات، جریان ایزنتروپیک جریان سیالی است که هم آدیاباتیک و هم برگشت پذیر است. به این معنا که هیچ گرمایی به جریان اضافه نمی شود و هیچ تغییر انرژی به دلیل اصطکاک یا اثرات اتلاف کننده رخ نمی دهد . برای یک جریان همسانتروپیک یک گاز کامل، چندین رابطه را می توان برای تعریف فشار، چگالی و دما در امتداد یک خط جریان به دست آورد.
توجه داشته باشید که انرژی را می توان با جریان در یک تبدیل ایزنتروپیک مبادله کرد، البته تا زمانی که به صورت تبادل حرارتی اتفاق نیفتد. نمونه ای از چنین تبادلی، انبساط یا فشرده سازی ایزنتروپیک است که مستلزم کار انجام شده روی جریان یا توسط جریان است.
برای یک جریان ایزنتروپیک، چگالی آنتروپی می تواند بین خطوط جریان مختلف متفاوت باشد. اگر چگالی آنتروپی در همه جا یکسان باشد، آنگاه گفته می شود که جریان همنتروپیک است.
اشتقاق روابط ایزنتروپیک [ ویرایش ]
برای یک سیستم بسته، کل تغییر انرژی یک سیستم مجموع کار انجام شده و گرمای اضافه شده است:
کار برگشت پذیری که روی یک سیستم با تغییر صدا انجام می شود
جایی که


سپس برای فرآیندی که هم برگشت پذیر و هم آدیاباتیک است (یعنی انتقال حرارت رخ نمی دهد)،

در مرحله بعد، مقدار زیادی را می توان برای فرآیندهای ایزنتروپیک یک گاز ایده آل محاسبه کرد. برای هر تبدیل گاز ایده آل، همیشه این درست است

با استفاده از نتایج کلی به دست آمده در بالا برای

بنابراین برای یک گاز ایده آل، نسبت ظرفیت گرمایی را می توان به صورت زیر نوشت
برای یک گاز کالری کامل
به این معنا که،
استفاده از معادله حالت برای گاز ایده آل
(اثبات:

همچنین برای ثابت

بنابراین برای فرآیندهای همسانتروپیک با گاز ایده آل،

جدول روابط همسانتروپیک برای یک گاز ایده آل [ ویرایش ]
ناشی شدن از
جایی که:













همچنین ببینید [ ویرایش ]
ریاضیات...برچسب : نویسنده : 9math1342d بازدید : 237
























